Good Documentation Practices (GDocP)
di tulis oleh Ariyono W Ardi , Drs. Apt. MM .pada 24 Oktober 2022
Good Documentation Practice (GDocP) adalah prosedur sistematis mulai dari persiapan, peninjauan, persetujuan, penerbitan, pencatatan, penyimpanan, dan pengarsipan dokumen.
Apakah Good Doc Practice (GdocP) itu….?
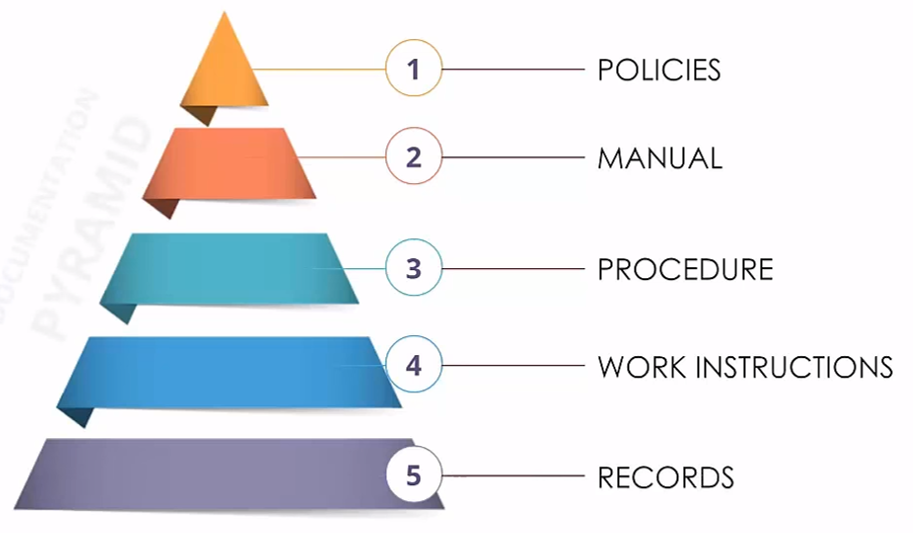
- Dokumen adalah informasi (data yang bermakna) dan media pendukungnya, berupa kertas, CD, file komputer, mikrofilm, film x-ray, dll.
- Dokumen memberikan informasi atau bukti atau dapat berfungsi sebagai catatan resmi.
- Record adalah dokumen yang menyatakan hasil yang dicapai atau memberikan bukti kegiatan yang dilakukan.
- Guideline/Pedoman adalah dokumen yang menggambarkan praktik dan instruksi yang direkomendasikan.
- Kebijakan (Policy) adalah rencana atau tindakan yang diadopsi atau prinsip tindakan yang dimaksudkan untuk mempengaruhi dan menentukan keputusan atau tindakan organisasi.
ADocuments Pyramid

Mengapa GdocP Sangat Penting Bagi Pelanggan?
- Beberapa pelanggan adalah perusahaan yang menerapkan aturan manajemen mutu secara ketat
- Kesalahan dokumentasi dapat menyebabkan konsekuensi yang kritis terkait dengan:
- Keamanan produk
- Proses pengadilan
- Pelanggaran dari aturan pemerintah
- Good Documentation Practices (GDocP) diperlukan dalam hal penjaminan kebenaran terhadap tindakan yang telah dilakukan vs SOP sebagai bukti pada saat audit
- GDocP berlaku untuk semua proses dokumentasi termasuk dalam system management mutu yang terus dikembangkan
- GMP adalah bagian dari jaminan kualitas yang memastikan bahwa produk secara konsisten diproduksi dan dikendalikan dengan standar kualitas yang sesuai untuk penggunaan yang dimaksudkan
- Dokumentasi juga merupakan kunci kepatuhan GMP karena memastikan ketertelusuran semua aktivitas mulai dari pengembangan, proses produksi, dan pengujian
- Dokumentasi merupakan sarana bagi auditor untuk menilai kualitas keseluruhan operasi dalam perusahaan dan produk akhir
- Dokumentasi juga merupakan kunci kepatuhan CPOB karena memastikan ketertelusuran semua aktivitas mulai dari pengembangan, proses produksi, dan pengujian
Prinsip-prinsip GDocP
- Dokumen dengan tanda tangan asli tidak boleh dimusnahkan.
- Jangan pernah memalsukan informasi
- Jangan menggunakan Tip-ex untuk mengganti kesalahan
- Jangan pernah melenyapkan informasi atau catatan
- Jangan menggunakan pensil untuk mengisi data/informasi
- Semua informasi harus ditulis dengan tinta Hitam atau Biru permanen
- Di dalam dokumen/record jangan ada ruang/kolom yang dibiarkan kosong.
- Jangan pernah menggunakan simbol misalnya tanda ditto atau panah untuk menunjukkan pengulangan aktifitas yang berturut-turut
- Hasil cetak komputer yang diambil di atas kertas termal atau tinta yang mudah pudar harus difotokopi dan dipelihara. Asli harus dimusnahkan setelah verifikasi
- GMP memerlukan bahwa dokumen hendaklah:
- Dikontrol dalam kerangka Sistem Manajemen Mutu
- Disetujui, ditandatangani dan tanggal
- Secara periodik harus direview
- Disimpan hingga waktu tertentu, dan
- Dapat diperbaharui dalam kerangka Sistem Manajemen Mutu.
- Jangan lakukan:
- Jangan hapus halaman atau bagian apa pun dari buku catatan (log book).
- Jangan membuat catatan sementara di secarik kertas atau di telapak tangan
- Pertahankan buku catatan tetap utuh
- Jangan membuat catatan di post-it®
- Jangan menyalin data
- Hindari penggunaan buku catatan laboratorium yang tidak teresgister
- Membuat ulang atau menulis ulang catatan harus dihindari
- Jika memang diperlukan, lakukan sebagai berikut:
- Persetujuan dari supervisor terkait dan QA
- Idintifikasi dokumen dengan “re-write”
- Catatan boleh ditulis ulang, hanya jika:
- Catatan asli bisa dibaca dengan jelas
- Formulir atau dokumen yang digunakan salah
- Catatannya bis adiperbaiki
- Catatan yang asli dalam format yang tidak bisa disimpan lama (thermal paper).
- Jika memang diperlukan, lakukan sebagai berikut:
- Witnessed/Checked/Reviewed by
- Ketika satu orang melakukan tugas dan orang kedua bertugas untuk memferifikasi bahwa itu tugas itu telah dilakukan dengan benar
- Pemeriksaan ganda memberikan jaminan tambahan bahwa tidak ada kesalahan yang dibuat
- Orang yang melakukan verifikasi harus jelas apa yang mereka verifikasi bubuhkan tanda tangan dan tanggal pada dokumen
Tipe-tipe Dokumen
- Spesifikasi
- Instruksi pengolahan dan pengemasan
- Standard operating procedures (SOP)
- Catatan yang terkait dengan kualitas.
- Technical agreements
- Confidentiality agreements
- Technical reports
- Dokumen-dokumen lain yang terkait dengan Quality Manajemen Mutu
- Laporan penyimpangan (Deviation reports)
- Audit plans
- Validation Master Plans dan validation documents termasuk URS, DQ, FAT, IQ, OQ, PQ, and Validation reports
- Dokumen yang terkait bahan uji termasuk spesifikasi produk, penerimaan bahan uji, dan laporan hasil uji.
- Dokumen yang terkait dengan karyawan, seperti: catatan training dan kesehatan karyawan.
- Personnel related documents including training records
- Change control
- Worksheets, notebooks, and logbooks
- Quality Manual
- SOP’s
- Validation protocols and reports
- Dokumen yang terkait dengan fasilitas, spt: spesifikasi lantai, HVAC dan lingkungan.
- Form Deviasi baik untuk deviasi yang tidak terencana dan Sistem Investigasi Kegagalan (system failure investigation)
- Kontrol Perubahan (Change control)
- Worksheets, notebooks, and logbooks
- Quality Manual
- SOP’s
- Validation protocols and reports
Karakteristik GDocP
The 8 Rules
- Permanen (Permanent)
- Informasi tidak dapat diubah, dihapus, atau dihilangkan
- Alat tulis yang benar (CPOB)
- Tidak boleh menggunakan pinsil
- Tinta permanen
- Hitam atau Biru
- Memberikan tampilan dan standar dokumen yang konsisten
- Alat tulis yang benar (CPOB)
- Informasi tidak dapat diubah, dihapus, atau dihilangkan
- Jelas terbaca (Legible)
- Informasi dapat dengan mudah dibaca
- Jika ada kesalahan, diperbaiki dengan benar
- Mencoret diatas tulisan asli
- Jangan lakukan:
- Coret atau hitamkan dengan pena
- White out
- Write over
- Jelaskan alasan kesalahan
- Tulis informasi yang benar
- Paraf dan tanggal
- Faktor-faktor yang harus diperhatikan:
- Keterbacaan angka dan karakter
- 0 and 6
- U and V
- 1 and 7
- 3 and 8
- B and 8
- Keterbacaan angka dan karakter
- Informasi dapat dengan mudah dibaca
- Akurat (Accurate)
- Perhitungannya benar dan informasi dicatat dengan hati-hati
- Lakukan perhitungan paling tidak Dua Kali
- Hendaklah perhitungan ditinjau dan diverifikasi oleh orang kedua
- Sajikan hasil dalam unit yang telah ditentukan ditentukan
- Penulisan nama produk sudah benar
- Nomor lot, nomor seri, dan kode produk diperiksa dua kali
- Perhitungannya benar dan informasi dicatat dengan hati-hati
- Segera (Prompt)
- Informasi dicatat pada waktu yang tepat. Tindakan didokumentasikan segera, tidak pernah sebelumnya
- Dokumentasikan aktifitas segera setelah dilakukan
- Jangan pernah melakukan dokumentasi sebelum atau sesudah tanggal!
- Jika Anda melewatkan satu langkah dalam suatu proses, jujurlah. Dokumentasikan dan selesaikan langkah pada saat itu jika memungkinkan, catat tanggal sebenarnya saat aktifitas itu selesai.
- Informasi dicatat pada waktu yang tepat. Tindakan didokumentasikan segera, tidak pernah sebelumnya
- Konsisten (Consistent)
- Lengkap (Complete)
- Semua informasi disertakan
- Tidak ada ruang, halaman, atau bagian halaman yang kosong
- N/A hanya dapat digunakan jika sangat jelas bahwa sebagian dari dokumen, formulir, catatan tidak berlaku.
- Berikan penjelasan dengan N/A (Contoh “N/A” dikarenakan pengujian diakukan berulang” Paraf dan Tanggal.
- Untuk tabel yang tidak digunakan, Tarik garis (“/”) pada tabel yang tidak digunakan, beri penjelasan dengan N/A, lalu paraf dan beri tanggal.
- Gambar garis “Z” pada halaman yang kosong dan tulis “blank”, paraf dan tanggal
- Semua informasi disertakan
- Langsung (Direct)
- Informasi dicatat segera ke formulir yang tepat, buku catatan laboratorium atau sistem komputer.
- Data asli isikan langsung ke dokumen GMP.
- Tidak ada catatan di kertas bekas dan ataupun post it (kertas tempel).
- Jangan menulis di wadah bahan baku, kardus, sarung tangan, dll.
- Informasi dicatat segera ke formulir yang tepat, buku catatan laboratorium atau sistem komputer.
- Sesuai kenyataan (Truthful)
- Informasi yang benar yang dicantumkan dalam dokumen adalah, adalah faktual.
- Tanda tangan/inisial Anda mengatakan bahwa informasi itu Benar
- Informasi yang Anda laporkan, harus faktual. Informasi tidak boleh dipalsukan
- Informasi yang benar yang dicantumkan dalam dokumen adalah, adalah faktual.
- Permanen (Permanent)
Karakteristik GDocp
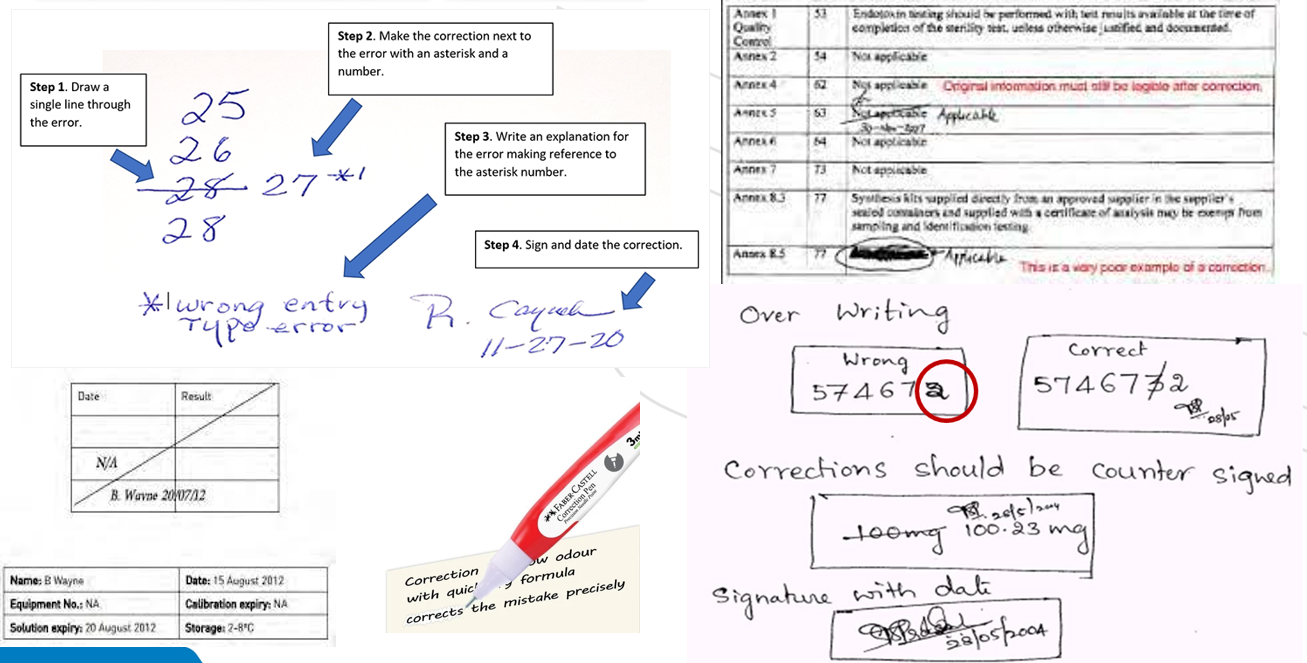
Contoh Penerapan GDocP
- Format tanggal
- Dokumentasi pada saat aktifitas dilakukan
- Setiap perubahan didokumentasikan
- Penyimpangan segera ditangani
- Koreksi dicatat secara efektif dan akurat
- Area kosong diidentifikasi dengan benar dan dengan penjelasan terdokumentasi.
Kesalahan Umum dalam Dokumentasi
- Tidak ada tanda tangan dan tanggal pada saat aktivitas dilakukan.
- Write-over
- Tanggal dan penulisan tanda tangan tidak seragam.
- Ruang kosong
- Tulisan yang tidak jelas terbaca
- Terlalu banyak koreksi
- Dokumentasi tidak segera dilakukan
- Penggunaan kata-kata “idem/dito” pada pekerjaan yang sama
- Menggunakan stampel tanda tangan
- Kegagalan menggunakan tinta seperti yang telah ditentukan oleh prosedur
- Koreksi buku catatan (logbook) gagal mengidentifikasi orang yang membuat perubahan
- Data asli yang tidak terbaca dengan jelas
- Penggunaan pensil
- Catatan yang tidak akurat
- Tabel urutan sampel dan jejak audit (audit trail) tidak didokumentasikan.
- Perubahan tulisan tangan tidak bertanggal
- Tulisan double, beberapa garis koreksi, dan penggunaan Tip-Ex or atau perangkat penyamaran lain.
- Koreksi kesalahan dokumentasi harus mencakup:
- Coret dengan satu garis diatas informasi yang salah,
- Tulis koreksi di sebelah kesalahan,
- Tulis penjelasan mengapa terjadi kesalahan,
- Paraf dan tanggal terhadap koreksi
Documents Management
- Setiap organisasi farmasi harus memiliki sistem untuk manajemen dokumentasi, yang berisi aturan dan mekanisme untuk membuat dan mengendalikan dokumen
- Menugaskan seseorang untuk tanggung jawab dalam mengendalikan system dokumentasi
- Memastikan tata letak (layout), persetujuan (approval), otorisasi (authorization), dan identifikasi unik dari semua dokumen yang terkait dengan kualitas yang terkontrol dalam Master SOP
- Memiliki Master Documentation SOP termasuk:
- Prosedur untuk penerbitan (issue) , penarikan, penerbitan ulang, pemeliharaan dokumen dan ketertelusurannya
- Sistem identifikasi dokumen termasuk batch manufacturing record
- Keterkaitan dokumen dengan dengan aturan-aturan pemerintah atau aturan cGMP yang lain.
- Diperlukan audit khusus untuk dokumentasi manajemen system.
- Jaminan bahwa hanya dokumen dengan versi terkini yang digunakan di lapangan.
- Waktu penyimpanan dan pengarsipan
- Document Control
- Dokumen harus tersedia di setiap titik penggunaan
- Master, termasuk versi elektronik, harus dikendalikan
- Ada pengawasan atas format dokumen
- Ada sistem untuk pengawasan perubahan, persetujuan, dan penerbitan ulang
- Ada pengawasan atas dokumen yang berasal dari luar
- Document Creation
- Dokumen harus up to date dengan peristiwa yang mereka gambarkan
- Dokumen tidak boleh ditulis tangan (kecuali data/informasi yang harus diisi manual)
- Ketika diproduksi secara elektronik, dokumentasi harus diperiksa keakuratannya
- Bebas dari kesalahan
- Untuk beberapa jenis data, dokumentasi harus dalam format yang memungkinkan untuk evaluasi data trend.
- Document Approval
- Dokumen harus disetujui untuk digunakan. Dokumen harus disetujui, ditandatangani, dan diberi tanggal oleh personel yang berwenang.
- Hand written entry
- Ruang yang memadai perlu disediakan untuk pengisian dengan tulisan tangan.
- Pengisian dengan tulisan tangan harus dengan tinta yang tidak terhapuskan
- Pengisian data-data kritis harus diperiksa secara independent (second person verified)
- Tidak ada ruang untuk pengisian tulisan tangan yang harus dibiarkan kosong. Jika ruang tidak digunakan, ruang kosong harus dicoret atau "n/a" (atau teks serupa). Penulisan Tanda “Ditto” tidak dapat diterima
- Stempel sebagai pengganti tanda tangan tulisan tangan tidak dapat diterima
- Document Copies
- Salinan harus jelas dan dapat dibaca
- Kesalahan tidak diperbolehkan
- Dokumen harus ditinjau secara teratur dan tetap terkini,
- Dokumen harus disimpan dan tersedia untuk audit
- Dokumen dalam arsip harus dapat diambil kembali selama durasi yang sesuai
- Sistem manajemen dokumen elektronik harus divalidasi
- Catatan elektronik harus digandakan sebagai “Back up”
- Document Modification
- Modifikasi tulisan tangan ditandatangani dan diberi tanggal
- Teks yang diubah tidak boleh dikaburkan
- Bila perlu, alasan perubahan harus dicatat
- Pengawasan untuk mencegah penggunaan dokumen lama secara tidak sengaja
- Electronic Record
- Kita dapat menggunakan sistem manajemen informasi laboratorium (LIMS) untuk merekam hasil test secara elektronik
- Sebagai formulir terkontrol yang dibuat dalam Microsoft Word (elektronik) hendaknya dicetak di atas kertas untuk diperiksa sehingga dapat ditandatangani untuk disetujui
- Document Storage
- Penyimpanan catatan penting harus di tempat yang aman, dengan akses terbatas hanya untuk orang yang berwenang
- Lokasi penyimpanan harus memastikan perlindungan yang memadai dari kehilangan, kehancuran, atau pemalsuan, dan dari kerusakan akibat kebakaran, air, dan bencana lainnya.
- Catatan yang penting untuk kepatuhan terhadap peraturan atau untuk mendukung kegiatan bisnis penting harus digandakan di atas kertas, mikrofilm, atau elektronik, dan disimpan di lokasi terpisah yang aman di gedung yang terpisah dari aslinya
Observation in Poor GDocP
- Tidak ada tanda tangan dan tanggal pada saat aktivitas dilakukan
- Tanggal dan tanda tangan tidak seragam
- Kegiatan dilakukan pada satu hari dan menandatangani pada hari lain
- Ruang kosong
- Tulisan yang tidak terbaca
- Terlalu banyak koreksi
- Tulisan tumpang tindih dan garis koreksi berulang-ulang
- Penggunaan perangkat penghapus
- Penggunaan pensil
- Koreksi kesalahan tidak ditandatangani dan diberi tanggal, dan alasan koreksi tidak ditulis
- Tidak dapat dilacak
- Integritas data diragukan