Kami membantu menyelaraskan kegiatan validasi proses dengan konsep siklus hidup produk dan dengan Pedoman FDA yang ada termasuk ICH-Q08 (Pengembangan Farmasi), ICH-Q09 (Manajemen Risiko Mutu) & ICH-Q10 (Sistem Mutu Farmasi).
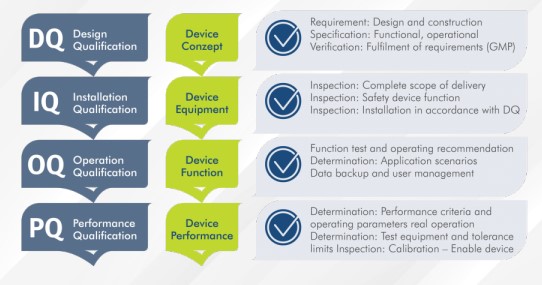
Layanan ini juga mencakup dukungan untuk mengembangkan Validasi Master Plan (VMP) dan dokumen terkait lainnya berdasarkan analisis berbasis risiko dan panduan untuk menerapkan Kualifikasi Desain (DQ), Kualifikasi Instalasi (IQ) dan Kualifikasi Operasional (OQ) termasuk tinjauan dan panduan untuk pelaksanaan dan pencatatan. Ini akan memastikan bahwa validasi dilaksanakan dengan lancar dan tanpa redundansi.